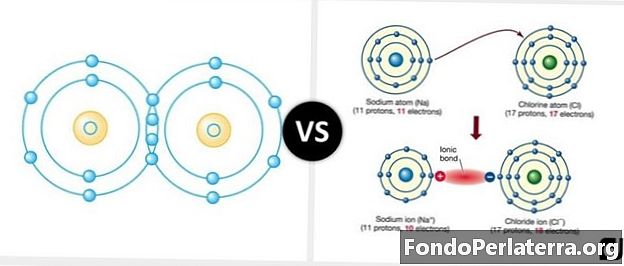
Covalente obligaties versus ionische obligaties
Inhoud
- Inhoud: Verschil tussen Covalent Bonds en Ionic Bonds
- Vergelijkingstabel
- Wat is Covalent Bonds?
- Wat is Ionische obligaties?
- Belangrijkste verschillen
Het belangrijkste verschil tussen ionische bindingen en covalente bindingen is het delen van elektronenparen en atomen. In covalente bindingen worden atomen elektrostatisch naar elkaar getrokken terwijl ze in ionische bindingen zijn; elektronenparen worden gedeeld tussen atomen.
Inhoud: Verschil tussen Covalent Bonds en Ionic Bonds
- Vergelijkingstabel
- Wat is Covalent Bonds?
- Wat is Ionische obligaties?
- Belangrijkste verschillen
- Video uitleg
Vergelijkingstabel
| Onderscheidingsbasis | Covalente obligaties | Ionische bindingen |
| Definitie | Een covalente binding is een soort chemische binding waarbij gedeelde paren of bindingsparen (elektronenparen) tussen atomen worden gedeeld. | Een ionische binding is het type chemische binding waarbij een of meer elektronen door een atoom met een ander atoom worden gedeeld of volledig worden opgegeven. |
| voorval | Covalente bindingen zijn het resultaat van interactie van neutrale atomen | Ionische bindingen zijn het resultaat van de interactie tussen anionen en kationen. |
| Chemisch potentieel | Dit zijn vrij zwakke chemische bindingen | Dit zijn het sterkste type chemische binding. |
| Vorming | Niet-metalen elementen vormen covalente bindingen | Metalen elementen vormen ionische bindingen |
| Elektronenstatus | Gedeelde elektronen | Totale overdracht van elektronen |
| De stand van zaken | Vloeistoffen en gassen bij kamertemperatuur | Vaste stoffen bij kamertemperatuur |
| verbindingen | Biologisch | Anorganisch |
| oplosbaarheid | Onoplosbaar in water | Oplosbaar in water |
| Vorm | Definitieve vorm | Geen definitieve vorm |
| Naming | Griekse voorvoegsels | Romeinse cijfers |
| Voorbeelden | Waterstofchloride en methaan | Zwavelzuur en natriumchloride |
Wat is Covalent Bonds?
Covalente bindingen, ook bekend onder de naam moleculaire bindingen, zijn het type chemische bindingen waarbij gedeelde paren of bindingsparen (elektronenparen) tussen atomen worden gedeeld. In de meeste moleculen zorgt de elektronen ervoor dat elk atoom het equivalent krijgt van een volledige buitenste schil, overeenkomend met een stabiele elektronische configuratie. Als atomen een vergelijkbare affiniteit voor elektronen hebben, zullen waarschijnlijk covalente bindingen optreden vanwege dezelfde affiniteit voor elektronen en geen neiging om ze door atomen te doneren. Atomen delen elektronen om een octetconfiguratie te krijgen en stabieler en sterker te worden. Vanwege interacties van de sigma- en pi-orbitalen kunnen covalente bindingen vier soorten bindingen vormen, namelijk enkele, dubbele, drievoudige en viervoudige. Zuurstofatomen zijn het beste voorbeeld dat twee extra elektronen vereist om een gesloten schaal te vormen, terwijl waterstofatomen er een nodig hebben om een gesloten schaal te vormen. Een zuurstofatoom deelt twee van zijn elektronen met waterstofatomen, dus de atomen van beide hebben gesloten omhulsels. Hierdoor ontstaat uiteindelijk een watermolecuul.
Wat is Ionische obligaties?
Een ionische binding is het type chemische binding waarbij een of meer elektronen door een atoom met een ander atoom worden gedeeld of volledig worden opgegeven. Ionische bindingen zijn het resultaat van die elementen die gemakkelijk elektronen verliezen en die elementen die elektronen winnen. Dit soort bindingen doen dat helemaal niet, moleculen vanwege de interactie tussen ladingen zoals beschreven in de wet van Coulomb. Ionische bindingen blijven vast bij kamertemperatuur omdat, tijdens periodieke roosters met miljarden ionen, elk ion wordt omringd door vele ionen van tegengestelde lading. De elektrostatische aantrekkingskracht tussen de negatieve en positieve ionen houdt de verbinding bij elkaar. De totale energie tijdens het ionbindingsproces is normaal positief, wat aangeeft dat de reactie endotherm en ongunstig is. Anderzijds is deze reactie tegelijkertijd gunstig vanwege hun elektrostatische aantrekkingskracht. Een gebruikelijk voorbeeld van een ionische binding is natrium of zout. Natriumatomen geven snel elektronen af die resulteren in een positieve lading. Chloor accepteert deze elektronen en is negatief geladen. Deze twee tegengesteld geladen atomen trekken elkaar dan aan om een natriumchloride-molecuul te vormen.
Belangrijkste verschillen
- In covalente bindingen overlappen elektronenorbitalen terwijl deze gescheiden zijn in het geval van ionische bindingen.
- Covalente bindingen zijn relatief zacht in vergelijking met ionische bindingen die hard en bros zijn.
- Zowel metaalatomen als niet-metaalatomen zijn betrokken bij de vorming van ionische bindingen tijdens de vorming van covalente bindingen; alleen niet-metalen atomen zijn betrokken.
- Covalente bindingen worden gevormd vanwege het delen van elektronen terwijl ionische bindingen ontstaan door het overbrengen van elektronen.
- Moleculen zijn de deeltjes in covalente bindingen tijdens de vorming van verbindingen, terwijl deze in ionische bindingen positief en negatief geladen ionen zijn.
- Covalente bindingen zijn niet-geleiders, terwijl ionische bindingen geleiders zijn.
- Covalente binding vindt plaats tussen atomen met weinig verschillende elektronegativiteit. Ionische binding vindt plaats tussen atomen met een groot verschil in elektronegativiteit.
- Ionische bindingen vereisen een hoog smeltpunt en een kookpunt in het geval van ionische binding. Covalente bindingen vereisen een laag smelt- en kookpunt in geval van covalente binding.
- Methaan en waterstofchloride zijn veel voorkomende voorbeelden van een covalent natriumchloride en zwavelzuur zijn voorbeelden van ionische bindingen.
- Covalente bindingen hebben een bepaalde vorm, terwijl ionische bindingen geen bepaalde vorm hebben
- Covalente bindingen hebben een lage polariteit, terwijl ionische bindingen een hoge polariteit hebben.
- 100% covalente moleculen lossen op in olie, maar niet in water, terwijl veel ionische bindingen kunnen oplossen in water maar niet in olie.
- Covalente bindingen zijn belangrijk omdat koolstofmoleculen primair op elkaar inwerken door covalente binding, terwijl ionische bindingen belangrijk zijn omdat deze de synthese van specifieke organische verbindingen mogelijk maken.
- Covalente bindingen kunnen zowel elementen als verbindingen zijn, terwijl ionische bindingen alleen verbindingen kunnen zijn.